A materialista

Dicas de Química!
Aqui você encontra dicas da matéria mais temida por todos: a química!
O que é Química ?

A Química é a ciência responsável por estudar a matéria e suas transformações.
Matéria

É tudo aquilo que tem massa e ocupa um lugar no espaço (ocupa um determinado volume).
Estados Físicos da Matéria

Os estados físicos da matéria são três: sólido, líquido e gasoso, são dependentes da temperatura e da pressão.
Estado Sólido

O estado sólido é um estado da matéria, cujas características são ter volume e forma definidos (isto é, a matéria resiste à deformação). Dentro de um sólido, os átomos ou as moléculas estão relativamente próximos, ou "rígidos".
Estado Líquido

Uma substância no estado líquido tem volume definido, mas não tem forma própria, tomando a forma do recipiente em que está contido.
Estado Gasoso

O estado gasoso é caracterizado por ter completa falta de rigidez, grande capacidade de expansão, podendo ocupar qualquer volume ao seu dispor.
Propriedades da Matéria

Massa: quantidade de matéria
Impenetrabilidade: dois corpos não ocupam o mesmo lugar
Compreensibilidade: a matéria pode ser comprimida
Volume: espaço ocupado pela matéria
Divisibilidade: pode ser dividido sem descaracterização
Propriedades Organolépticas

As características que são perceptíveis aos sentidos humanos: cor, brilho, odor e textura.
Fenômenos Físicos

São as transformações da matéria que resultam apenas na troca de estado físico (sólido, líquido, gasoso) sem que ocorra alteração na composição química da matéria.
Exemplo: solidificação, transformação da água em estado líquido para estado sólido
Fenômenos Químicos

São transformações na matéria que resultam na formação de novas substâncias, ou seja, ocorre a mudança na composição química da matéria.
O átomo!

O átomo é a unidade básica da matéria.
Sendo divido em núcleo (prótons e nêutrons) e eletrosfera (elétrons).
Elemento Químico

O elemento químico é caracterizado pelo seu número atômico, cujo símbolo é Z. O número atômico é o número de prótons que esse elemento contém.
A massa atômica é o soma do número de prótons e nêutrons. Ou seja, A= p + n
Isótopos, Isóbaros e Isótonos

Isótopos: átomos com mesmo número atômico, porém diferente massa.
Isóbaros: átomos com diferente número atômico, porém mesma massa.
Isótono: mesmo número de nêutrons, porém diferente número atômico e diferente massa.
Elétrons

Os elétrons são partículas de carga negativa que ficam dispostas em camadas eletrônicas: K, L, M, N, O, P e Q.
Diagrama de Linus Pauling

Os elétrons são distribuídos de acordo com o diagrama de Linus Pauling.
A distribuição dos elétrons se inicia sempre pelas camadas 1s/2s/2p/3s.
Para ter a explicação completa sobre distribuição eletrônica clique aqui!
Átomo eletricamente neutro, cátion e ânions.

Eletricamente Neutro: é um átomo que possui a mesma quantidade de prótons e elétrons.
Cátion: é um íon com carga positiva, devido a perda de elétrons.
Ânion: é um íon com carga negativo, devido ao ganho de elétrons.
Tabela Periódica

A Tabela Periódica é um modelo que agrupa todos os elementos químicos conhecidos (118 elementos: 92 naturais e 26 artificias) e suas propriedades. Eles estão organizados em ordem crescente de número atômico (número de prótons).
Substâncias Simples e Substâncias Compostas

Substâncias Simples: as moléculas são constituídas por um único elemento químico. Exemplo: He
Substância Composta: são moléculas ou compostos iônicos formados por mais de um elemento químico. Exemplo: H2O
Substância Pura e Mistura

Substância Pura: é aquela que compreende um único tipo de constituinte que possui propriedades física e químicas próprias.
Mistura: é a união de duas ou mais substâncias puras. Por essa razão, por exemplo, não possuem ponto de fusão e ebulição específicos.
Classificação das Misturas

Homogêneas: não conseguimos observar a divisão entre seus componentes.
Heterogêneas: mistura composta por mais de uma fase, ou seja, é possível observar a divisão entre componentes.
Azeotrópica: possuem ponto de ebulição/condensação constante como se fosse um substâncias pura
Eutética: possuem ponto de fusão/solidificação constante como se fosse um substâncias pura.
Suspensão: misturas heterogêneas que conseguimos identificar as fases a olho nu.
Colóide: misturas heterogêneas que não conseguimos identificar as fases a olho nu. Exemplo: gelatina.
Propriedades Coligativas

O conteúdo sobre solução está no final dessa apresentação.
São propriedades de uma solução que apenas têm relação com a quantidade de soluto dissolvido, não importando a natureza do soluto em si.
Tonoscopia: redução da pressão de vapor do solvente em razão da adição do soluto.
Quanto maior a pressão de vapor de um líquido, mais volátil ele é.
Ebulioscopia: elevação do ponto de ebulição pela adição de um soluto não volátil ao solvente.
Crioscopia (ou abaixamento crioscópico): redução da temperatura de congelamento dada a presença de partículas de soluto.
Osmose: é o fluxo de solvente através de uma membrana para uma solução mais concentrada. Tal membrana deve ser seletiva (semipermeável), de modo a permitir a passagem do solvente, mas não do soluto.
Métodos de Separação

Decantação: separa misturas heterogêneas (L+L ou S+L) de acordo com a densidade dos componentes.
Centrifugação: utiliza o processo de centrifuga para acelerar a decantação.
Dissolução Fracionada: um líquido dissolve um dos sólidos em uma mistura heterogênea. A mistura então é filtrada (recuperação do primeiro sólido) e depois aquecida para recuperação do segundo sólido.
Destilação Homogênea: aquecimento de um mistura para separação do sólido/líquido. O líquido é recuperado devido a presença de um condensador no sistema.
Destilação Fracionada: separação da mistura de líquidos baseada na diferença do ponto de ebulição dos mesmo.
Filtração: é um método utilizado para separar sólido de líquido que está suspenso, utilizando um meio permeável capaz de reter as partículas sólidas.
Flotação: separação de misturas que consiste na introdução de bolhas de ar a uma suspensão de partículas. Com isso, verifica-se que as partículas aderem às bolhas, formando uma espuma que pode ser removida da solução, o que permite separar seus componentes de maneira efetiva.
Levigação: separação de misturas heterogêneas de sólidos. Quando uma mistura se forma por substâncias sólidas de densidades diferentes, pode-se utilizar uma corrente de água para separá-las.
Ligações Químicas

Iônicas: ligação química ocorre entre cátions e ânions.
Covalente: ligação química que ocorre pelo compartilhamento de elétrons da camada de valência
Metálicas: ocorre apenas entre os átomos de um único metal e exclusivamente porque um metal não pode estabelecer ligação química com outro elemento metálico diferente.
Moléculas Polares x Moléculas Apolares

Polares: devido a uma diferença de eletronegatividade, forma-se um polo negativo e um polo positivo. Lembre-se molécula polar dissolve molécula polar.
Apolares: não existe diferença de eletronegatividade entre os elementos. São solúveis em moléculas polares.
Exemplo: água (polar) e óleo (apolar) formam um sistema heterogêneo bifásico.
Alotropia

Alotropia é o fenômeno que ocorre quando um elemento químico forma duas ou mais substâncias simples diferentes.
A alotropia ocorre da atomicidade (exemplo o O2 (gás oxigênio) e O3 (ozônio)) ou da distribuição dos átomos no espaço (como exemplo o carbono, na imagem acima).
A forma de distribuição dos átomos confere ao material diferentes propriedades, o grafite é mole e usado em lápis, enquanto o diamante é o material mais duro que se conhece.
Forças Intermoleculares

São as forças necessárias para manter unidas duas o mais moléculas.
Ligação de Hidrogênio: ligação de forte intensidade. Ocorre em moléculas polares que tem o hidrogênio ligado a elementos eletronegativos (Oxigênio, Flúor, Cloro). Exemplo: ligação ocorre entre as moléculas de água no estado líquido e sólido.
Dipolo Permanente: ligação de média intensidade. é uma força intermolecular que ocorre em substâncias polares. Os polos contrários da moléculas se atraem.
Dipolo Induzido: ligação de fraca intensidade. É uma atração intermolecular que ocorre entre uma substância polar e apolar ou apolar-apolar.
Ácido

Ácido é toda substância que em uma solução aquosa sofre dissociação iônica e gera como único cátion o íon H+.
São líquidos a temperatura ambiente e tem pH inferior a 7.
Para saber mais sobre a ácidos, bases e pH clique aqui!
Base

A base é uma substância que em solução aquosa sofre uma dissociação iônica e gera o ânion hidroxila, OH-.
pH

pH é a sigla para potencial de hidrogênio. É utilizado como uma escala que indica: acidez, neutralidade ou alcalinidade de uma substância. A escala varia de 0 até 14.
pH < 7 - pH ácido - a concentração de cátions H+ é maior que a do ânion OH-
pH = 7 - pH neutro
pH > 7 - pH básico - a concentração de cátions H+ é menor que a do ânion OH-.
14 = pH + pOH.
NOX - Número de Oxidação

É a carga elétrica que um elemento adquire quando faz uma ligação iônica ou a carga parcial quando faz uma ligação covalente.
Lembre-se: alguns elementos tem NOX fixo, outros tem NOX variáveis.
Os elementos eletronegativos tem tendência a NOX negativo.
Os elementos eletropositivos tem tendência a NOX positivo.
Outras Substâncias

Óxidos: é uma substância química formada por dois elementos sendo um deles o oxigênio.
Sais: é uma substância que produz , por dissociação iônica, uma cátions diferente de H+ e um ânion diferente de OH-.
Reações Químicas

Reações Inorgânicas: ocorrem entre substancias inorgânicas colocadas em um mesmo recipiente e que geram produtos diferentes dos reagentes iniciais.
Reações de Neutralização: ocorrem entre um ácido e uma base, sendo o produto final sal e água,.
Simples Troca: é a reação entre uma substância simples e um substância composta. Os produtos da reação são uma outra substância composta e uma outra substancia simples.
Dupla Troca: são reações em duas substâncias compostas reagem entre si formando duas outras substâncias compostas.
Decomposição: aquelas em quem uma substância composta forma duas ou mais substâncias
Reação de Síntese: são aquelas em que duas ou mais substâncias simples formam uma substância composta.
Reação de Oxiredução: é uma reação em que acontece a mudança no NOX do elemento. Um elemento sofrerá oxidação (perderá elétrons) e o NOX aumentará. O outro elemento sofrerá redução (ganhará elétrons) e o NOX diminuirá.
Mol

Mol é uma unidade de medida que expressa a quantidade de átomos, íons e moléculas que uma determinada quantidade de uma substância qualquer contém.
1 mol equivale 6,02x10²³ átomos, íons ou moléculas.
1 mol de gás ocupa 22,4 L.
Lei de Proust e Lei de Lavoisier

Prost: Ela dispõe que quando dois ou mais elementos químicos se combinam mantém uma proporção em números inteiros que é constante.
Lavoisier:
Sistema Fechado: trata-se de um sistema em que não há fluxo de entrada e saída de partículas, ou seja, sua quantidade é constante.
A massa inicial do sistema é igual a massa final. Essa regra se aplica a todos os sistemas (fechados, abertos ou isolados).
Constante de Equilíbrio dos Gases

A constante do equilíbrio em termos de pressões parciais (Kp) é calculada com a divisão do produto entre as pressões dos produtos da reação pelos seus reagentes.
Kp = pressão do produto/pressão parcial dos reagentes
Deve-se levar em consideração o índice de cada gás envolvido na reação (olhar a imagem acima).
Pressão Total (Pt) é a soma de todas as pressões parciais.
Pt = Preagentes + Pprodutos
Para mais sobre Gases Ideais clique aqui!
Química Orgânica

É o segmento da química que estuda os compostos que possuem carbono e suas propriedades caraterísticas.
Proteínas, Lipídios, Carboidratos, gasolina, medicamentos, petróleo, entre outros caracterizam substâncias desse grupo.
Agente Oxidante e Agente Redutor

Agente Redutor: é a substância que sofre oxidação ou perda de elétrons.
Agente Oxidante: é a substância que sofre redução ou ganho de elétrons.
Pilhas

As pilhas são componentes que produzem energia elétrica a partir de energia química. São processo espontâneos em que a DDP é positiva.
É necessária a presença de um cátodo (polo positivo), um ânodo (polo negativo) e uma ponte salina.
Eletrolise

A eletrólise é um processe não espontâneo (DDP Negativa) que precisa de uma fonte de energia para funcionar.
A eletrólise pode ser ígnea ou aquosa.
É necessária a presença de um cátodo (polo negativo), um ânodo (polo positivo) e uma bateria ou um retificador.
Para saber mais sobre eletroquímica clique aqui!
Corrosão

É um processo de oxiredução em que um determinado metal sofrerá deterioração, ou oxidação, devido a presença de intempéries no meio (agente oxidantes como água e oxigênio).
Quando dois metais estiverem em contato, o metal mais susceptível a corrosão é aquele com menor potencial de redução (maior potencial de oxidação).
Entalpia
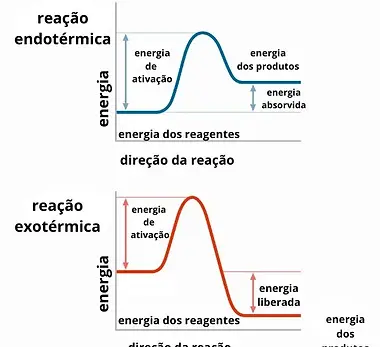
É a parte da química que estuda a energia interna (calor) que os reagentes e os produtos de uma reação química possuem.
Reações exotérmicas são aquelas que liberam calor. A variação de entalpia é menor que zero. Exemplo: combustão.
Reações endotérmicas são aquelas que absorvem calor. A variação de entalpia é maior que zero. Exemplo: reação de decomposição da água.
Lei de Hess

Essa lei permite o cálculo da entalpia das substâncias com base nas reações intermediárias.
Medidas e Unidades

Massa: 1 kg = 1000g
Comprimento: 1 m = 100 cm
Tempo: segundos (s)
Temperatura: kelvin (K)
T(K) = T (°C) + 273,15 T(°F) = (9/5)T(°C) + 32
Volume: litro (L) = 1000mL
Pressão: pascal, Pa (N/m²); 1 atm = 101,325 Pa
Força: newtom, N = kg.m/s²
Carga: Coulom, C
Energia: joule, J (kg m²/s²) = 0,23901 cal




